Typ
Datum
89 Ergebnisse

SGS beim EMV Kongress in Köln – vom 12. bis 14. März 2024
Auch in diesem Jahr stellen wir mit unseren Fachexperten auf dem EMV Kongress vom 12. - 14. März in Köln wieder Beiträge und Workshops vor.
Mehr lesen
Künstliche Intelligenz und Funktionale Sicherheit im Automotive Sektor
Mit dem Seminar „Kompakteinstieg - Vertrauenswürdige KI im Automotive Bereich“ launchen SGS-TÜV Saar und das Fraunhofer-Institut für Intelligente Analyse- und Informationssysteme (IAIS) am 12. Dezember 2023 erstmals ein Schulungsangebot, das Führungskräfte und technisches Fachpersonal grundlegend für den Einsatz Künstlicher Intelligenz fit machen soll. Referenten des eintägigen Seminars sind Dr. Michael Mock (Projektleiter bei IAIS und Privatdozent an der Uni Bonn) und Eduard Dojan (Product Manager Software & Artificial Intelligence, SGS-TÜV Saar).
Mehr lesen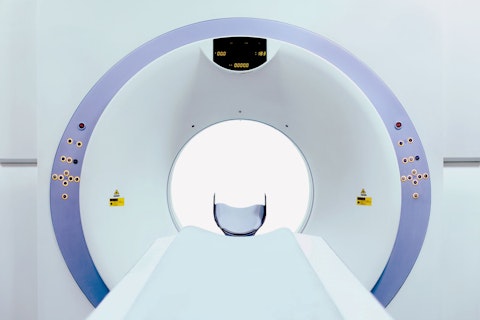
Treffen Sie uns auf der MEDICA 2023
Sie möchten Ihr Medizinprodukt nach MDR prüfen und zertifizieren lassen und dabei nicht durch lange Wartezeiten ausgebremst werden oder erwägen als Medizinproduktehersteller einen Wechsel Ihrer Benannten Stelle?
Mehr lesen
Rundum-Lösung für nachhaltiges Bauen und Modernisieren
Die SGS Gruppe Deutschland und das Sentinel Haus Institut verstärken ihre Kooperation: Gemeinsam wollen die Unternehmen einen 360°-Ansatz bei der Beratung und Prüfung von gesünderen und kreislauffähigen Bauprodukten und Gebäuden etablieren.
Mehr lesen
Änderungen im vereinfachten Eisenbahnversandverfahren (vgVV) endet, die Lösung: digitales NCTS Verfahren durch SGS TransitNet
Das bisherige Zollverfahren vgVV wird im Laufe des Jahres 2023 schrittweise ungültig - SGS bietet das NCTS-Versandverfahren über TransitNet und weitere Zolldienstleistungen wie ABD-Erstellung und Importverzollungen an.

Die SGS beim EMV-Kongress 2023 in Stuttgart – 28. bis 30.03.23
Auch 2023 stellen wir mit unseren Fachexperten Armin Hudetz, Josef Bauer, Markus Spiel und Michael Sperling vom 28. bis 30.03. auf dem EMV-Kongress in Stuttgart interessante Workshops vor.

SGS begrüßt proderm in der SGS Gruppe Deutschland
Nach der erfolgreichen Übernahme der proderm GmbH, dem führenden Anbieter von fortschrittlichen klinischen Testlösungen für Kosmetika, Körperpflegeprodukte, dermatologische Arzneimittel und Medizinprodukte in Deutschland, im Juli 2022, konnten wir im Dezember 2022 die Umfirmierung in SGS proderm GmbH vollziehen. Mit diesem wichtigen Schritt sind wir künftig in der Lage, unseren Kunden unser vollumfassendes Portfolio als Einheit anzubieten und gemeinsam stark am Markt aufzutreten zu können. Wir freuen uns, mit SGS proderm eine neue Marke innerhalb unserer Gruppe begrüßen zu dürfen.
Mehr lesen
Neue und aktuelle Schulungen zu den Themen SOTIF, KI und Cyber Sicherheit (bei SGS-TÜV-Saar)
Das Thema Funktionale Sicherheit entwickelt sich in rasendem Tempo weiter. Gerade hat sich die Anwendung der ISO 26262 im Automotive Bereich etabliert und schon stößt man damit an die Grenzen der Anwendbarkeit. SOTIF, KI und Cyber Sicherheit sind die neuen Schlagworte, die den Innovationen im Bereich des hoch automatisierten Fahrens zu einer ungeahnten Dynamik verhelfen.
Mehr lesen
IT-Sicherheit in der Automobilbranche: SGS-TÜV Saar GmbH erhält „TISAX®“-Label
TISAX® gilt als aktueller Standard für den Nachweis der Informationssicherheit in der Automobilbranche. Hersteller verlangen von ihren Zulieferern und Dienstleistern immer häufiger einen entsprechenden Nachweis. Durch einen bei der ENX Association gelisteten Prüfdienstleister (DQS) hat SGS-TÜV Saar GmbH - als Unternehmen des weltgrößten Prüf- und Zertifizierdienstleisters SGS mit ihren 96.000 Mitarbeitern - das TISAX® -Assessment nach TISAX® -Spezifikationen gemäß VDA-ISA erfolgreich absolviert.
Mehr lesen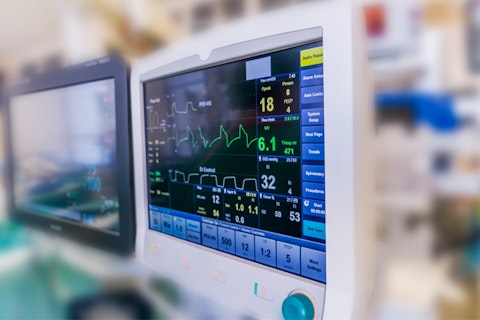
Die SGS auf der MEDICA 2022 in Düsseldorf (14. - 17. November)
Die Experten der SGS – Weltmarktführer im Bereich Testen, Prüfen und Zertifizieren – informieren Sie auf der weltweit größten Veranstaltung für die Medizinbranche, wie Sie Ihre Medizinprodukte international erfolgreich in Verkehr bringen und welche Normen und Verordnungen Sie einhalten müssen.
Mehr lesen